- إنضم
- 25 يناير 2015
- المشاركات
- 1,527
- مستوى التفاعل
- 6,849
- النقاط
- 113
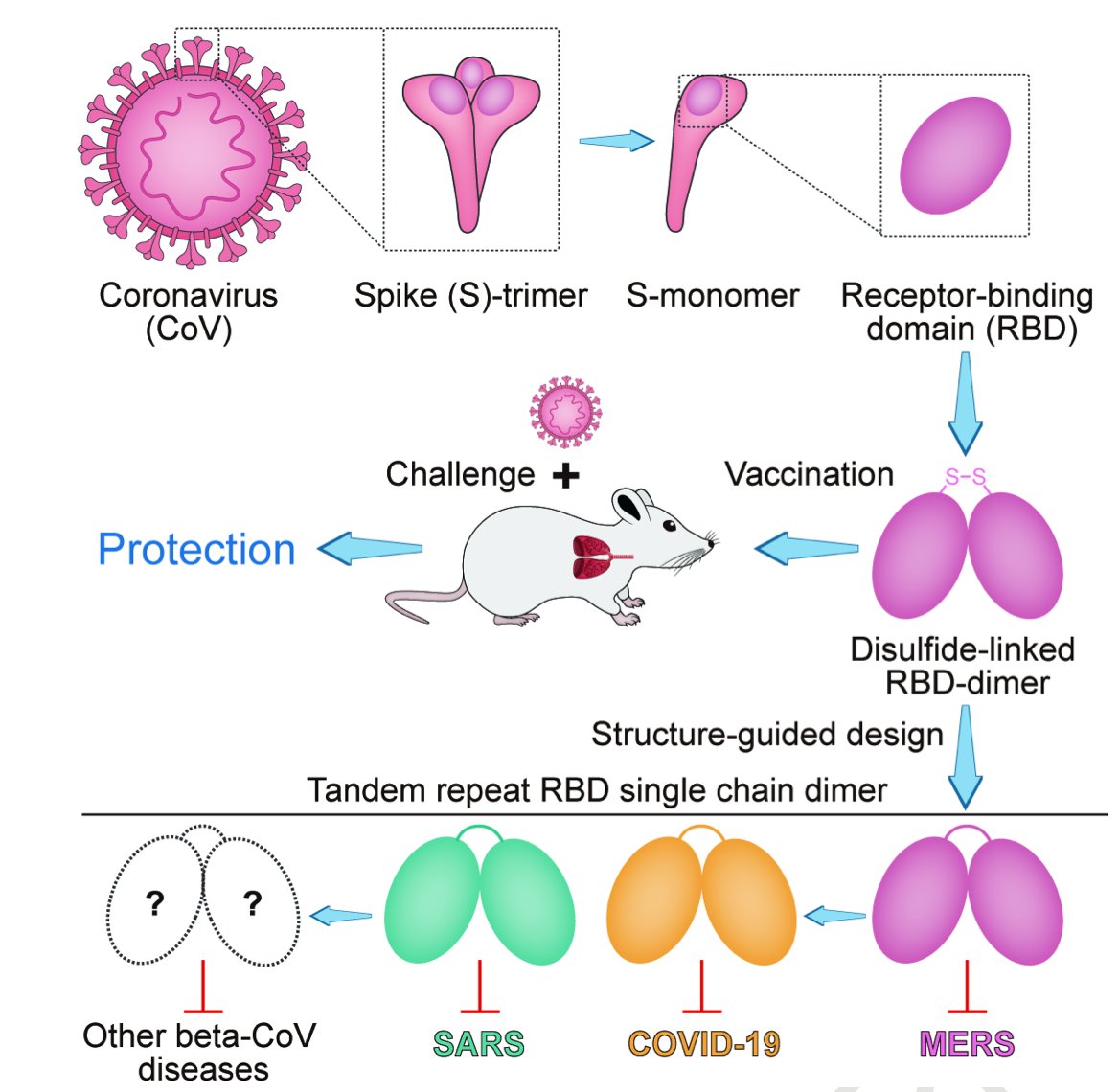
لقاح Recombinant subunit بتقنية Recombinant DNA لإستخدام مع المساعد التقليدي RBD كمستضد ل spike glycoprotein المسؤول عن الإلتحام مع مستقبل المضيف لكن ليس بشكل احادي بل ثنائي او دايمر الذي تم تحسين تصميمه ليكون أكثر ثباتا وتجانس فتم الحصول علي دايمر احادي السلسلة RBD تكراري ترادفي RBD-sc-dimer للتغلب علي محدودية الاستمناع او لزيادة بشكل كبير من تركيز neutralizing antibody ب 10 - 100 ضعف والذي يتم إنتاجه من خلايا CHO لمعهد الميكروبيولوجي للأكادمية الصينية للعلوم CAS ولشركة Chongqing Zhifei Biological Products تم الموافقة عليه للبدء بالتجارب السريرية من إدارة المنتجات الطبية الصينية NMPA بعد إثبات تاثيره الوقائي علي الفئران المعدلة وراثيا والمكاك الريسوسي والتلقيح أدي لمستويات عالية من neutralizing antibodies وكما يخفض لحد كبير من الحمل الفيروسي بانسجة الرئة والذي يقلل من تلف الرئة الناجم من العدوي الفيروسية والمرحلة الاولي من التجارب السريرية ستبدأ في مستشفي The Second Affiliated لجامعة تشونغتشينغ الطبية CQMU ومستشفي Beijing Chaoyang لجامعة Capital Medical في بكين .
智飞生物重组新型冠状病毒疫苗启动Ⅱ期临床试验
تم إطلاق المرحلة الثانية من التجارب السريرية للقاح أثنين من الوحدة الفرعية البروتينية التي بتحتوي كل منها علي RBD للسبايك لشركة Anhui Zhifei Longcom Biopharmaceutical ومعهد الميكروبيولوجي لأكادمية الصين للعلوم CAS في مركز شيانغتان بمقاطعة هونان للوقاية من الامراض ومكافحتها لتقييم السلامة والاستمناع بشكل أوسع مع 900 شخص بعد البدء بالمرحلة الاولي من التجارب السريرية مع 50 شخص .
لقاح كوفيد-19 S-Trimer او SCB-2019 لشركة Clover Biopharmaceuticals بدأ المرحلة الاولي من التجارب السريرية كسادس مرشح صيني بالتجارب السريرية فتم تطعيم المشاركين الأوائل من ضمن 150 حيث 90 من البالغين الاصحاء و 60 من كبار السن الاصحاء لدراسة السلامة وإحداث التفاعل المعاكس والاستمناع في Linear Clinical Research ببيرث بأستراليا ضمن دراسة عمياء وهمية أي إعطاء اللقاح لأشخاص لتقييمه وأخرين بالبلاسيبو أي بيتم إيهامهم نفسيا ان تم تطعيمهم ومزدوجة التعمية وعشوائية وبيتم تقييم اللقاح بجرعات مختلفة بأثنين من adjuvant حيث مساعد CpG 1018 بالشب لشركة Dynavax الأمريكية أو بمساعد GSK البريطانية الذي أثار مع لقاح SCB-2019 مستويات عالية من الأجسام المضادة المحايدة في الحيوانات والنتائج ستكون في أغسطس وبيتم التخطيط لتجربة 2b/3 لدراسة فاعلية اللقاح بنهاية العام وعلماء شركة Clover Biopharmaceuticals في مطلع عام 2020 بدأوا في تصميم بروتين s الفيروسي وأتموا توليف الجينات وبتقنية Trimer-Tag© الحاصلة علي براءة إختراع أنتجت Clover لقاح الوحيدات COVID-19 S-Trimer المرشح الذي يماثل بروتين سبايك ثلاثي الوحدات بالغلاف الفيروسي ومساعد من شركة GlaxoSmithKline البريطانية سيتوفر للقاحات الوحيدات الأخري الصينية المطورة من Anhui Zhifei Longcom Biopharmaceutical التابعة لشركة Chongqing Zhifei Biological Products وكذلك لشركة Xiamen Innovax Biotech التي بالتقييمات قبل السريرية والمساعد ضروري لتقليل من كمية البروتينات المطلوبة لكل جرعة لإمكانية إنتاج جرعات أكبر من اللقاح وإتاحته لمزيد من الناس .
للقاح SCB-2019 تلقت شركة Clover Biopharmaceuticals تمويل إضافي بحوالي 66 مليون دولار للدراسات قبل السريرية وتنفيذ المرحلة الاولي من التجارب السريرية والتخطيط لتجارب التحقق من الفاعلية ولزيادة القدرة التصنيعية لمئات الملايين من الجرعات سنويا من تحالف ابتكارات التأهب الوبائي CEPI الذي يذكر انه سبق وقدم دعما ماليا بحوالي 3.5 مليون دولار للإعداد وإطلاق المرحلة الاولي من التجارب السريرية .
معهد البيوتكنولوجى التابع ل AMMS سبق وطور مع شركة CanSino Biologics بتيانجين اللقاح القائم علي فيروس الغدي المؤتلف Ad5-nCoV الذي خاض المرحلة الثانية من التجارب السريرية بووهان وأخذ الموافقة بالبدء بالتجارب السريرية بكندا لان الفيروسات رائعة في غزو الخلايا والتي منها بيسمح لها بالتكاثر كالأنفلونزا كناقل RBD بلقاح جامعة هونج بالتقييم قبل السريري والتي لا يسمح لها بالتكاثر كالفيروس الغداني Ad5 كناقل كما بلقاح Ad5-nCoV او Ad26 كما بلقاح Johnson & Johnson وبيلاحظ ان الاستمناع يكون أقوي ب Ad5 فعادتاً بيكون تركيزات neutralizing antibody ل Ad26 منخفضة جدا عند المقارنة لكن هذا ياتي علي حساب العائق امام التمنيع المتتالي ب Ad5 كما مشكلة وجود مناعة مسبقا حيث تم الإصابة مؤخرا بفيروس الفيروس الغداني البشري 5 فحيث معظم جزيئات الفيروس تتعرض للهجوم من جهاز المناعة قبل ان تتمكن من توصيل حمولتها للخلية حيث كمثال من خلال التسلسل الجيني لبروتين سبايك ل sars cov-2 بيتم إحداث شريط من الحمض النووي لترميز بروتين سبايك وبيتم إستنساخه في الفيروس الغدي الناقل الذي يوصل الجين للخلية لكي يتعرف الجسم علي بروتين سبايك ويذكر ان في لقاحات بتقوم علي فيروس غدي غير بشري كناقل حيث بالشمبانزي المعتمد ب ChAdOx1 لجامعة أكسفورد وهو بيتخلص من مشكل وجود مناعة مسبقا لان من يستضيف الفيروس ليس الإنسان لكنه لم يستخدم من قبل في لقاح والحمل الفيروسي عند تلقيح المكاك الريسوسي يذكر انه إنخفض بالجهاز التنفسي السفلي لكن لم يلاحظ إنخفاضه بالانف فهوا بيوقف تفاقم المرض فهوا هكذا سيكون لقاح علاجي مع الملاحظة انك بتحتاج لجرعة واحدة تقريبا تريليون من جزيئات الفيروسية غير مشكل التبريد فصعب الإعتماد علي لقاح Ad5-nCoV بفيروس الغداني البشري كناقل حتي بعد أن تثبت فاعليته لتلقيح عشرات او مئات الملايين .
تم نشر نتائج المرحلة الاولي من التجارب السريرية للقاح Ad5-nCoV المطور من معهد بكين للتكنولوجيا الحيوية وشركة CanSino Biologics بتيانجين حيث 108 من المتطوعين بأعمار بين 18-60 في ووهان و 36 لكل مجموعة للجرعات الخفيفة والمتوسطة والعالية وتم ملاحظة 83 % من مجموعات الجرعات الخفيفة والمتوسطة و 75 % للجرعة العالية أبلغوا عن رد فعل سلبي واحد علي الاقل في غضون 7 أيام حيث 58 من 108 أي بنسبة 54 % أبلغوا عن ألم بمكان الحقن و 50 من 108 أي بنسبة 46 % كان لديهم حمي و 47 من 108 أي 44 % كان لديهم إعياء و 42 من 108 أي بنسبة 39 % صداع و 18 من 108 أي بنسبة 17 % ألم عضلي لكن الحمي بتختفي في 48 ساعة فبعد التطعيم ب 28 يوم لم يلاحظ أي ردود فعل سلبية مهمة فاللقاح ظهر انه امن وتم ملاحظة ان لقاح الجرعة العالية كان اكثر توليد مناعة من متوسط ومنخفض الجرعة لكنه أيضا كان مرتبط بالقدرة علي إحداث ردود فعل سلبية أعلي حيث حمي شديدة وإعياء وضيق بالتنفس والام عضلية وبالمفاصل في بعض متلقي الجرعات العالية وحيث عاني منهم 21 من 36 أي بنسبة 58 % ألم بمكان الحقن و 20 من 36 أي 56 % من الحمي و17 من 36 أي 47 % من الصداع و 16 من 36 أي 44 % إعياء و 8 من 36 أي بنسبة 22 % لالم عضلي و 6 من 36 أي 17 % ضعف بالشهية و 5 من 36 أي 14 % إسهال ولالم بالمفاصل لكن معدل الإستجابة كان يقارب 100 % وتم ملاحظة الإستجابات الخلطية ذروتها في اليوم 28 والخلايا التائية T-cell في اليوم 14 بعد التطعيم فتم التحقق أيضا من قدرة إنتاج الأجسام المضادة المحايدة وإستجابة الخلايا التائية باللقاح الذي قائم علي منهج الناقل الفيروسي والذي فيه non-replicating كما لقاح Ad5-nCoV القائم علي الفيروس الغدي الضعيف بجانب replicating كاللقاح القائم علي الانفلونزا Influenza vector expressing RBD لجامعة هونغ كونغ الذي لم يدخل بعد التجارب السريرية .
First human trial of COVID-19 vaccine finds it is safe and induces rapid immune response
جرعة واحدة من لقاح Ad5-nCoV في غضون أسبوعين أثارت الإستجابة المناعية في شكل إرتباط الأجسام المضادة بالمستقبلات الفيروسية التي يمكن ان ترتبط بفيروس كورونا لكن ليس من الضروري ان تهاجمه ل 16 من 36 مشارك بمجموعة الجرعة المنخفضة أي بنسبة 44 % و 18 من 36 مشارك بمجموعة الجرعة المتوسطة أي بنسبة 50 % و 22 من 36 مشارك بمجموعة الجرعة العالية أي بنسبة 61 % وكذلك بالنسبة للأجسام المضادة المحايدة لفيروس SARS-CoV-2 حيث 10 من 36 مشارك بمجموعة الجرعة المنخفضة أي بنسبة 28 % و 11 من 36 مشارك بمجموعة الجرعة المتوسطة أي بنسبة 31 % و 15 من 36 مشارك بمجموعة الجرعة العالية أي بنسبة 42 % . باليوم 28 يوم بعد التطعيم حصل زيادة بأربعة أضعاف للأجسام المضادة التي ترتبط بالمستقبلات الفيروسية للمشاركين بالتجربة السريرية ب 35 من 36 مشارك بمجموعة الجرعة المنخفضة أي بنسبة 97 % و 34 من 36 مشارك بمجموعة الجرعة المتوسطة أي بنسبة 94 % و 36 من 36 مشارك بمجموعة الجرعة العالية أي بنسبة 100 % وللأجسام المضادة المحايدة لفيروس SARS-CoV-2 ب 18 من 36 مشارك بمجموعة الجرعة المنخفضة ونفس الامر بالجرعة المتوسطة أي بنسبة 50 % و 27 من 36 مشارك بمجموعة الجرعة العالية أي بنسبة 75 % . حفز أيضا لقاح Ad5-nCoV الخلايا التائية التي بلغت ذروتها في اليوم 14 حيث 30 من 36 مشارك بمجموعة الجرعة المنخفضة أي بنسبة 83.3 ٪ و 35 من 36 مشارك بكل مجموعة للجرعة المتوسطة والعالية أي بنسبة 97.2 % . باليوم 28 بعد التطعيم ظهر إستجابة إيجابية للخلايا التائية ضد فيروس SARS-CoV-2 ب 28 من 36 مشارك بمجموعة الجرعة المنخفضة أي بنسبة 78 % و 33 من 36 مشارك بمجموعة الجرعة المتوسطة أي بنسبة 92 % و 36 من 36 مشارك بمجموعة الجرعة العالية أي بنسبة 100 % .
يمكن أن تبطئ الإستجابة المناعية ل SARS-CoV-2 ومستوي الذروة للخلايا التائية والأجسام المضادة بتقل عند الأشخاص من لديهم مناعة عالية مسبقا من ناقل فيروس البرد الشائع أي adenovirus type 5 أي للاشخاص الذين إصيبوا بنزلات البرد ويلاحظ أن 44-56 % من شاركوا بالتجربة السريرية للقاح Ad5-nCoV كان لديهم هذه المناعة العالية ومع ذلك بالتقدم بالتجارب السريرية والبحث من المنتظر أن نعرف هل الإستجابة المناعية الضعيفة لمثل هولاء الأشخاص تؤثر بشكل كبير علي التأثير الوقائي للقاح أم لا .
CanSino's recombinant COVID-19 vaccine approved as special military drug
CanSino had previously announced in May that the Canadian government was allowing human trials of the Ad5-nCoV vaccine. "This vaccine candidate holds great promise," Iain Stewart, president of the National Research Council of Canada, said in a statement at the time
تمت الموافقة علي لقاح Ad5-nCoV القائم علي الفيروس الغداني Ad5 الذي ينقل للخلايا جين بروتين سبايك من معهد البيوتكنولوجى التابع لأكادمية العلوم الطبية العسكرية AMMS بالإشتراك مع شركة CanSino Biologics للإستخدام العسكري لمنع وعلاج الأمراض لمدة عام بعد نتائج المرحلة الثانية من التجارب السريرية التي أظهرت امان جيد ومستويات عالية للإستجابات المناعية الخلطية والخلوية و Ad5-nCoV ظهر بالمجمل انه بيمنع الامراض التي يسببها SARS-CoV-2 والذي سبق وتم السماح له بالتجارب السريرية في مايو بكندا والذي قال عليه مدير المجلس الوطني للبحوث بكندا Iain Stewart انه يحمل وعدا كبيرا .
China's CanSino in talks for COVID vaccine Phase III trial overseas
Vaccine promised for human trials in Canada held up by Chinese customs
China’s CanSino in talks for large-scale trial of potential coronavirus vaccine overseas
Canada yet to receive vaccine candidate from Chinese developer it reached an agreement with in May
CanSinoBIO, leading Covid-19 vaccine developer from China, joins hands with AJM Pharma Pakistan
Experts say side effect of COVID-19 vaccine tolerable, dismiss pessimism of West media reports
لم تبدأ التجارب السريرية بكندا للقاح Ad5-nCoV لشركة CanSino Biologics الصينية برغم الموافقة عليه وذلك بسبب الجمارك الصينية وهذا من خلال الصحة الكندية ومع ذلك بيذكر ان التجارب بكندا ستبدأ قريبا بمجرد الإنتهاء من الحصول علي الموافقات النهائية ... شركة CanSino Biologics الصينية لديها مصنع تحت الإنشاء لقدرة إنتاجية سنوية تصل من 100 - 200 مليون جرعة بدء من عام 2021 وقد وقعت مذكرة تفاهم مع AJM Pharma باكستان للتعاون بلقاح كوفيد-19 وبتتواصل كذلك مع روسيا والبرازيل وتشيلي والمملكة العربية السعودية لإطلاق بها المرحلة الثالثة من التجارب السريرية التي يرجح أن تبدأ قريبا جدا بمخطط بتجنيد حوالي 40 ألف شخص ... المتطوعين الذين تم تلقيحهم الأثار الضارة كانت خفيفة إلي متوسطة وليست خطيرة في 28 يوم بعد التطعيم والحمي إختفت في 48 ساعة والردود الفعل السلبية الاخري إختفت في 14 يوم بعد الحقن وبتذكر الشركة ان النتائج للسلامة والإستجابة المناعية للمرحلة الثانية بمشاركة 508 متطوع كانت افضل بكثير من المرحلة الاولي بمشاركة 108 متطوع .
لقاح كوفيد-19 المعطل لمعهد ووهان للمنتجات البيولوجية ل Sinopharm الذي خاض المرحلة الاولي والثانية من التجارب السريرية التي بدأت في 12 أبريل بمقاطعة خنان سيتدأ المرحلة الثالثة من التجارب السريرية للتأكد من فاعلية اللقاح في ووهان وبكين وأبو ظبي بعد ما تم إصدار الموافقة من عبدالرحمن بن محمد العويس وزير الصحة ووقاية المجتمع وهذا بشراكة بين CNBG التابعة ل Sinopharm ومجموعة 42 بأبوظبي .
لقاح الفيروس الكامل المشتق من خلايا الفيرو المستخلصة من القرود الافريقية الخضراء المقتول كيميائيا لمعهد بكين للمنتجات البيولوجية ل Sinopharm ظهرت النتائج الأولية للمرحلة الاولي والثانية التي بدأت في 27 أبريل بمقاطعة خنان بوسط الصين حيث أن جميع الملقحون بأثنين من الجرعات المنخفضة والمتوسطة والعالية لديهم اجسام مضادة بتركيز عالي بمعدل تحويل مصلي ل neutralizing antibodies وصل إلي 100 % علي أساس 0 و 21 يوم و 0 و 28 يوم وهذه التجارب الهدف منها هي التأكد من السلامة واللقاح بالفعل ظهر انه امن أي لم يكن هناك أي ردود فعل سلبية خطيرة بجانب الاستمناع او الحث لإستجابة مناعية مع التركيز علي مراقبة تغييرات المناعة الخلوية بعد التطعيم ومستويات الأجسام المضادة ل 1120 من الاشخاص الاصحاء باعمار بين 18-59 عاما ولمعهد بكين مرفق إنتاج بقدرة 120 مليون جرعة سنوية .
"They have entered the Phase III on clinical trials, and they are asking Bio Farma for joint research and production," Coordinating Ministry for Maritime Affairs and Investment spokesman Jodi Mahardi told Jakarta Globe's sister publication Suara Pembaruan on Monday
مجموعة الصين الدوائية Sinopharm و G42 بابوظبي الذين دخلوا المرحلة الثالثة من التجارب السريرية علي اللقاحات المعطلة عرضوا علي شركة Bio Farma باندونيسيا المشاركة بالبحث وكذلك بالإنتاج طبقا للمتحدث بإسم وزارة التنسيق للشؤون البحرية والاستثمار باندونيسيا .
أعلنت شركة Sinovac عن النتائج الاولية للتجارب السريرية بالمرحلة الاولي والثانية للقاح المعطل المرشح لكوفيد-19 بالمسمي التجاري CoronaVac حيث 143 متطوع بالمرحلة الاولي و 600 بالمرحلة الثانية ولم يتم الإبلاغ عن أي أثار ضارة خطيرة ل 743 شخص ونتائج التجارب السريرية للمرحلة الثانية تظهر أن تم إنتاج الأجسام المضادة المحايدة في 14 يوم نتيجة التطعيم بمعدل أعلي من 90 % ومن المنتظر ان تقدم الشركة تقرير عن الدراسة السريرية للمرحلة الثانية وبرتكول الدراسة السريرية للمرحلة الثالثة لإدارة المنتجات الطبية الصينية NMPA وبدء تطبيق المرحلة الثالثة للتجارب السريرية خارج الصين فيذكر أن في 11 يونيو تم توقيع إتفاقية تعاون بين الشركة ومعهد Butantan في ساو باولو بالبرازيل للإعداد وإجراء دراسية سريرية للمرحلة الثالثة بتجريبه علي 9000 متطوع بشهر يوليو والبرازيل بتستعد لإنتاجه ومع إختتام المرحلة الاولي والثانية بالنتائج المشجعة بالصين قرر الرئيس التنفيذي Weidong Yin لشركة Sinovac Biotech بالإستثمار في بناء منشأة تصنيع للقاح بالصين ب 100 مليون جرعة من CoronaVac سنويا .
Sinovac COVID-19 Vaccine Collaboration with Butantan Receives Approval from Brazilian Regulator for Phase III Trial
شركة SinoVac بلقاح المعطل CoronaVac الذي يحتوي علي مستضد فيروس SARS-COV2 غير نشط من خلايا vero مع كلوريد الصوديوم وفوسفات الهيدروجين ثنائي الصوديوم وفوسفات ثنائي الهيدروجين الصوديوم وهيدروكسيد الألمنيوم كمساعد بمشاركة معهد Butantan حصلوا علي موافقة الوكالة الوطنية للمراقبة الصحية بالبرازيل Anvisa واللجنة الوطنية لأخلقيات البحث Conep وستبدا المرحلة الثالثة من التجارب السريرية ب 9000 متطوع في 20 يوليو في 6 ولايات برازيلية .
التعديل الأخير: